La enorme importancia del agua WFI
Agua para preparaciones inyectables (WFI) es un tipo de agua especial que se utiliza en la fabricación de medicamentos parenterales, productos biológicos y dispositivos médicos. Debido a su contacto directo o indirecto con el torrente sanguíneo, la seguridad del agua para inyección (WFI) es primordial e innegociable en la industria farmacéutica.
El principal desafío: por qué el agua para inyección (WFI) es más difícil de controlar
A diferencia del agua purificada (PW), el agua WFI debe cumplir con una norma excepcionalmente estricta, centrada principalmente en dos contaminantes insidiosos:
- Contaminación microbiana:La presencia de bacterias viables.
- Endotoxinas bacterianas (pirógenos):Fragmentos de lipopolisacáridos inactivos que se desprenden de las paredes celulares de las bacterias gramnegativas muertas. Son muy difíciles de eliminar y pueden provocar fiebre y un shock pirogénico mortal en los pacientes.
Definición de seguridad: la norma reglamentaria
Un sistema de agua WFI solo se considera seguro cuando cumple sistemáticamente con los límites establecidos por las principales farmacopeas mundiales, como la Farmacopea de los Estados Unidos (USP) y la Farmacopea Europea (EP).
| Parámetro | USP [C<1231] | EP [0169] | Importancia de la seguridad |
| Conductividad | Máx. 1,3 µS/cm | Máx. 1,3 µS/cm | Control de iones y sales inorgánicas. |
| Límite microbiano (UFC) | Máx. 10 UFC/100 ml | Máx. 10 UFC/100 ml | Control de organismos viables. |
| Endotoxinas bacterianas | Max 0,25 EU/ml | Max 0,25 EU/ml | El límite crítico para la seguridad del paciente. |
La regla de oro de la producción de agua para inyección (WFI): el proceso de purificación con barreras múltiples
Para obtener agua WFI segura es necesario un proceso robusto de varias etapas en el que cada unidad actúe como una barrera a prueba de fallos contra las impurezas.
La primera barrera: el pretratamiento
La función principal del pretratamiento es proteger los equipos de purificación posteriores, que son más costosos. Por lo general, esto implica:
- Ablandamiento:Eliminación de la dureza (Ca²⁺ y Mg²⁺) para evitar la formación de incrustaciones en las membranas de ósmosis inversa y las unidades de destilación.
- Descloración:El uso de filtros de carbón activado para eliminar el cloro residual, que puede deteriorar las membranas de ósmosis inversa de compuesto de película delgada (TFC).
- Filtración de partículas:Eliminación de sólidos en suspensión que podrían obstruir el sistema.

La segunda barrera: purificación y desionización del núcleo
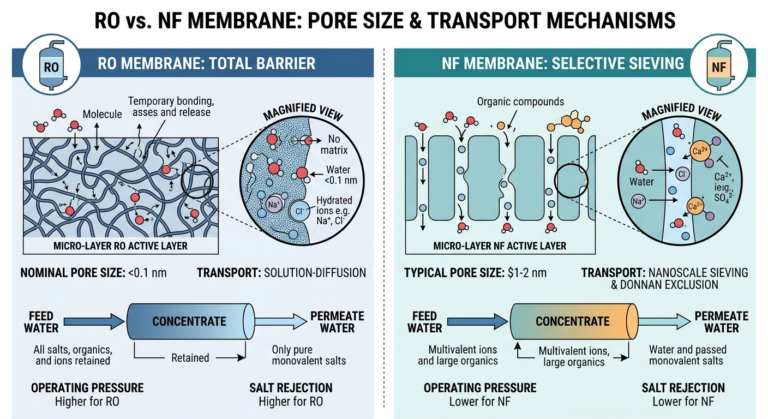
El núcleo del proceso de purificación es la ósmosis inversa.
El papel de la ósmosis inversa (RO): La ósmosis inversa (RO) es muy eficaz para eliminar entre el 95 % y el 99 % de las sales inorgánicas, las moléculas orgánicas de mayor tamaño y la mayoría de los contaminantes microbiológicos, transformando el agua de origen en agua purificada (PW) de alta calidad.
La tercera barrera: eliminación final de endotoxinas y bacterias (el paso crítico)
Esta es la etapa decisiva para garantizar la seguridad del agua WFI, concretamente la reducción drástica de las endotoxinas.
| Característica | Método tradicional: destilación de efectos múltiples (MED) | Método moderno: sistema basado en membranas (RO2/EDI/UF) |
| Mecanismo | El agua se hierve hasta convertirse en vapor y luego se condensa. Las impurezas no volátiles (sales, endotoxinas) permanecen en el depósito de ebullición. | Ósmosis inversa de doble paso (RO2) para una mayor eliminación, seguida de desionización eléctrica (EDI) para la desionización y, por último, Ultrafiltración (UF) como barrera física contra las endotoxinas. |
| Eficacia de la endotoxina | Excelente. Una reducción demostrada del nivel de log gracias a la separación física del vapor de las sustancias no volátiles. | Excelente. La ósmosis inversa y la membrana de ultrafiltración garantizan una eliminación constante y de alta eficacia. |
| Situación reglamentaria | Exigido por el Farmacopea Europea (EP) para la producción de agua WFI. | Aceptable por el Farmacopea de los Estados Unidos (USP) como método equivalente. |
| Ventajas | Probado a lo largo del tiempo, máxima fiabilidad, resistente a las variaciones en el agua de alimentación. | Menor consumo de energía, menor huella ecológica y validación más sencilla de la pureza mediante RO/EDI. |
El mayor riesgo del sistema de agua para inyección (WFI): el control del biofilm y del almacenamiento
Incluso el agua WFI perfectamente purificada puede dejar de ser segura si el circuito de almacenamiento y distribución se ve afectado por la reaparición de microorganismos y la consiguiente formación de biopelículas.
Circuito caliente frente a circuito frío: comparación de estrategias de control microbiano
La elección del método de almacenamiento es el factor determinante fundamental para la seguridad microbiana a largo plazo:
| Sistema | Circuito de distribución en caliente (método recomendado) | Circuito de distribución de frío |
| Temperatura | Normalmente se mantiene entre 65℃ y 80℃. | Conservar a temperatura ambiente (por ejemplo, 20℃-25℃). |
| Ventaja en materia de seguridad | La temperatura elevada constante actúa como un agente desinfectante térmico, lo que inhibe drásticamente el crecimiento microbiano y la colonización de biopelículas. | Requiere ciclos de desinfección programados y periódicos, ya sean químicos (por ejemplo, con ozono) o térmicos, para eliminar los microbios. |
| Riesgo | Alto costo energético. | Mayor riesgo de contaminación microbiana y de recrecimiento entre ciclos de desinfección. |
Elementos clave de seguridad en el diseño de sistemas de distribución
Para evitar el estancamiento —el principal caldo de cultivo para la contaminación microbiana—, el sistema debe estar diseñado por expertos:
Principio de «Zero Dead Leg» (ZDL): Cualquier ramal que conduzca a un punto de uso (POU) debe reducirse al mínimo. El tramo de tubería desde el circuito principal hasta la válvula del POU no debe tener una longitud superior a seis veces el diámetro del tubo de derivación. Esto garantiza que siempre circule agua WFI fresca.
Dinámica de fluidos: El sistema debe diseñarse para que alcance una velocidad suficiente y flujo turbulento (alto número de Reynolds) para evitar la sedimentación de partículas e inhibir la adhesión de microorganismos a las paredes de la tubería (el acero inoxidable 316L con acabado electropulido es el estándar).

Demostración continua de la seguridad del agua para inyección (WFI): validación y monitoreo
Un sistema de agua para inyección (WFI) seguro requiere una prueba documentada de que funciona, lo que se conoce como validación. Esto cumple con los requisitos normativos de E-E-A-T (experiencia, autoridad y fiabilidad).
El método de validación en tres pasos (IQ/OQ/PQ)
La validación es un proceso formal que demuestra el rendimiento constante del sistema:
- Calificación de la instalación (IQ):Comprueba que el equipo esté instalado correctamente y que cumpla con las especificaciones.
- Calificación operativa (OQ):Demuestra que el sistema funciona correctamente dentro de los rangos de funcionamiento previstos.
- Calificación de rendimiento (PQ):La fase crítica: demuestra, a lo largo de un período de tiempo (por ejemplo, 12 meses), que el sistema produce de manera constante agua WFI que cumple todos los requisitos de la farmacopea en condiciones de carga normal.
Supervisión de parámetros críticos de rendimiento (CPP)
La seguridad se garantiza mediante pruebas continuas y periódicas:
Supervisión en línea: Carbono orgánico total (TOC) y Conductividad se supervisan continuamente en línea. Una desviación en cualquiera de estos parámetros indica un fallo en las barreras de purificación (por ejemplo, una membrana de ósmosis inversa defectuosa o una pila de EDI averiada).
Estrategia de muestreo: Se deben tomar muestras de agua de rutina en los puntos designados Ubicaciones de muestreo en el peor de los casos. Esto incluye la línea de retorno (donde la carga microbiana suele ser más elevada) y la línea de punto de uso más larga y más alejada, con el fin de demostrar la seguridad en todo el circuito de distribución.
Buenas prácticas
Para responder de forma definitiva “¿Cómo garantizar la seguridad del agua WFI?” En el ámbito farmacéutico, es necesario adoptar un enfoque holístico basado en la calidad desde el diseño.
Seguridad de la WFI = Purificación de alta eficiencia (ósmosis inversa + destilación/membrana) + Control térmico continuo + Diseño optimizado de la línea de distribución (ZDL) + Validación rigurosa y documentada.
Al poner en práctica estas estrategias integradas, las instalaciones pueden mantener un Sistema de agua WFI que no solo cumple con las normas reglamentarias, sino que garantiza el máximo nivel de seguridad para los pacientes.