L'extrême importance de l'eau WFI
Eau pour injection (WFI) est une qualité d'eau spécialisée utilisée dans la fabrication de médicaments parentéraux, de produits biologiques et de dispositifs médicaux. En raison de son contact direct ou indirect avec la circulation sanguine, la sécurité de la WFI est primordiale et non négociable au sein de l'industrie pharmaceutique.
Le défi principal : pourquoi le WFI est plus difficile à contrôler
Contrairement à l'eau purifiée (PW), l'eau WFI doit répondre à des normes exceptionnellement strictes, ciblant principalement deux contaminants insidieux :
- Contamination microbienne :La présence de bactéries viables.
- Endotoxines bactériennes (pyrogènes) :Fragments de lipopolysaccharides non vivants libérés par les parois cellulaires des bactéries Gram négatives mortes. Ces fragments sont très difficiles à éliminer et peuvent provoquer de la fièvre et un choc pyrogène mortel chez les patients.
Définir la sécurité : La norme réglementaire
Un système d'eau WFI n'est considéré comme sûr que s'il respecte systématiquement les limites fixées par les principales pharmacopées mondiales, telles que la pharmacopée américaine (USP) et la pharmacopée européenne (EP).
| Paramètres | USP [C<1231] | EP [0169] | Importance de la sécurité |
| Conductivité | Max 1.3µS/cm | Max 1.3µS/cm | Contrôle des ions inorganiques/sels. |
| Limite microbienne (CFU) | Max 10CFU/100mL | Max 10CFU/100mL | Contrôle des organismes viables. |
| Endotoxines bactériennes | Max 0,25UE/mL | Max 0,25UE/mL | La limite critique pour la sécurité des patients. |
La règle d'or de la production de WFI : Le processus de purification à barrières multiples
L'obtention d'une eau WFI sûre nécessite un processus robuste en plusieurs étapes où chaque unité agit comme une barrière à sécurité intégrée contre les impuretés.
La première barrière : Le prétraitement
La fonction première du prétraitement est de protéger l'équipement de purification en aval, plus coûteux. Cela implique généralement
- Adoucissement :Élimination de la dureté Ca^2+ et Mg^2+ pour éviter l'entartrage des membranes d'osmose inverse et des unités de distillation.
- Déchloration :Utilisation de filtres à charbon actif pour éliminer le chlore résiduel, qui peut dégrader les membranes d'osmose inverse à couche mince (TFC).
- Filtration des particules :Élimination des matières en suspension susceptibles d'encrasser le système.

La deuxième barrière : Purification et déionisation de la carotte
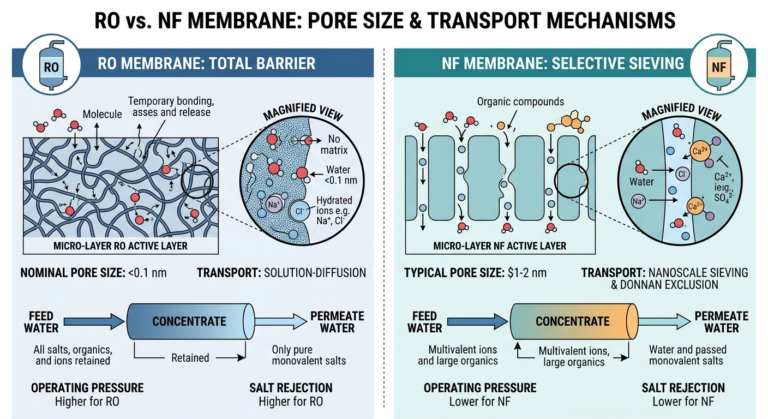
Le cœur du processus de purification est l'osmose inverse.
Le rôle de l'osmose inverse (OI) : L'OI est très efficace pour éliminer 95-99% des sels inorganiques, des molécules organiques plus grosses et la plupart des contaminants microbiologiques, transformant ainsi l'eau de source en une eau purifiée (EP) de haute qualité.
La troisième barrière : L'élimination finale des endotoxines et des bactéries (l'étape critique)
Il s'agit de l'étape décisive pour atteindre la sécurité de l'eau WFI, en particulier la réduction spectaculaire des endotoxines.
| Fonctionnalité | Méthode traditionnelle : Distillation à effets multiples (MED) | Méthode moderne : Système à membrane (RO2/EDI/UF) |
| Mécanisme | L'eau est bouillie et transformée en vapeur, puis condensée. Les impuretés non volatiles (sels, endotoxines) restent dans le bassin d'ébullition. | OI à double passage (OI2) pour une meilleure élimination, suivie d'une électro-désionisation (EDI) pour la déionisation, et enfin.., Ultrafiltration (UF) pour une barrière physique contre les endotoxines. |
| Efficacité contre l'endotoxine | Excellent. Une réduction prouvée des logs grâce à la séparation physique des vapeurs et des non-volatiles. | Excellent. L'OI et la membrane UF assurent une élimination constante et de haut niveau. |
| Statut réglementaire | Exigée par la Pharmacopée européenne (PE) pour la production d'eau WFI. | Acceptable par la Pharmacopée américaine (USP) comme méthode équivalente. |
| Pour | Testé dans le temps, la plus haute autorité, résistant aux variations de l'eau d'alimentation. | Consommation d'énergie plus faible, encombrement réduit, validation plus facile de la pureté RO/EDI. |
Le plus grand risque du système WFI : le biofilm et le contrôle du stockage
Même une eau parfaitement purifiée peut devenir dangereuse si la boucle de stockage et de distribution est compromise par la prolifération microbienne et les conséquences qui s'ensuivent. formation de biofilm.
Boucle chaude ou boucle froide : Comparaison des stratégies de contrôle microbien
Le choix de la méthode de stockage est le facteur déterminant de la sécurité microbienne à long terme :
| Système | Boucle de distribution chaude (méthode préférée) | Boucle de distribution de froid |
| Température | Généralement maintenue entre 65℃ et 80℃. | Stockés à température ambiante (par exemple, 20℃-25℃). |
| Avantage sécurité | La température élevée continue agit comme un agent d'assainissement thermique, drastically inhibiting microbial growth and biofilm colonization. | Nécessite des cycles de désinfection chimique (par exemple, à l'ozone) ou thermique programmés et périodiques pour éliminer les microbes. |
| Risque | Coût énergétique élevé. | Risque accru de contamination microbienne et de repousse entre les cycles d'assainissement. |
Principaux éléments de sécurité de la conception des réseaux de distribution
Pour éviter la stagnation - l'incubateur par excellence de la contamination microbienne - le système doit être conçu de manière experte :
Principe de la jambe morte zéro (ZDL) : Tout embranchement menant à un point d'utilisation (POU) doit être réduit au minimum. Le segment de tuyau entre la boucle principale et la vanne du point d'utilisation ne doit pas être plus long que six fois le diamètre du tuyau de dérivation. Cela permet de garantir que de l'eau fraîche WFI circule en permanence.
Dynamique des flux : Le système doit être conçu pour assurer une vitesse et un débit suffisants. flux turbulent (nombre de Reynolds élevé) pour empêcher la sédimentation des particules et la fixation des microbes sur les parois du tuyau (l'acier inoxydable 316L avec une finition électropolie est standard).

Preuve continue de la sécurité de l'IFW : Validation et surveillance
Un système WFI sûr nécessite une preuve documentée de son fonctionnement, appelée validation. Cela répond à l'exigence réglementaire E-E-A-T (Expertise, Autorité, Fiabilité).
La méthode de validation en trois étapes (IQ/OQ/PQ)
La validation est un processus formel démontrant la cohérence des performances du système :
- Qualification de l'installation (QI) :Vérifie que l'équipement est installé correctement et qu'il correspond aux spécifications.
- Qualification opérationnelle (OQ) :Prouve que le système fonctionne correctement dans les plages de fonctionnement prévues.
- Qualification des performances (PQ) :L'étape critique - elle démontre, sur une période de temps (par exemple, 12 mois), que le système produit régulièrement de l'eau WFI qui répond à toutes les exigences pharmacopées dans des conditions de charge normales.
Surveillance des paramètres critiques de performance (CPP)
La sécurité est assurée par des tests continus et périodiques :
Surveillance en ligne : Carbone organique total (COT) et Conductivité sont surveillés en permanence en ligne. Une excursion de l'un ou l'autre paramètre indique une défaillance des barrières de purification (par exemple, une membrane d'osmose inverse ou une pile EDI défaillante).
Stratégie d'échantillonnage : Les échantillons d'eau de routine doivent être prélevés à des endroits désignés. Lieux d'échantillonnage dans le pire des cas. Cela inclut la ligne de retour (où la charge microbienne est généralement la plus élevée) et la ligne la plus longue et la plus éloignée du point d'utilisation, afin de prouver la sécurité de l'ensemble de la boucle de distribution.
Meilleures pratiques
Pour répondre définitivement “Comment rendre l'eau WFI sûre ?” pour un usage pharmaceutique, il faut adopter une approche holistique de la qualité par la conception.
Sécurité WFI = Purification à haut rendement (RO + Distillation/Membrane) + Contrôle thermique continu + Conception ZDL optimisée + Validation rigoureuse et documentée.
En mettant en œuvre ces stratégies intégrées, les établissements peuvent maintenir un niveau de sécurité élevé. Système d'eau WFI qui non seulement répond aux normes réglementaires, mais garantit également le plus haut niveau de sécurité pour les patients.